刀尖上行走的临床设计!聊聊adc的安全窗口
2023-04-30
来源: drugdu
 4,141
4,141
big生物创新社
以下文章来源于新药说 ,作者sponge x
adc也好,化药也好,总说“肿瘤的临床往往都是在刀尖上走”,这个刀尖就是指的临床上安全窗口(therapeutic window)太小,我们看数据的时候,也总能看到“产品的安全窗口比阳性药扩大了几倍”来证明自己的产品更好。
本篇我们以zymeworks近期发表的一些数据来聊一聊安全性这个事情。
01 第一个问题,安全窗到底是什么?我们先把这个概念明确
mtd即maximum tolerated dose,指最大耐受剂量;med, minimum effective dose,最小有效剂量。介于这两者中间的即为安全窗口了,安全窗口越大,意味着留出的给药的空间就更大,有效性自然也就容易上去了。
另外一个常提到的为rp2d (recommended phase 2 dose 2 dose)剂量,即临床ii期的推荐剂量,看概念也能看出来,rp2d一般介于mtd和med中间,出于有效性考虑,往往更接近于mtd。
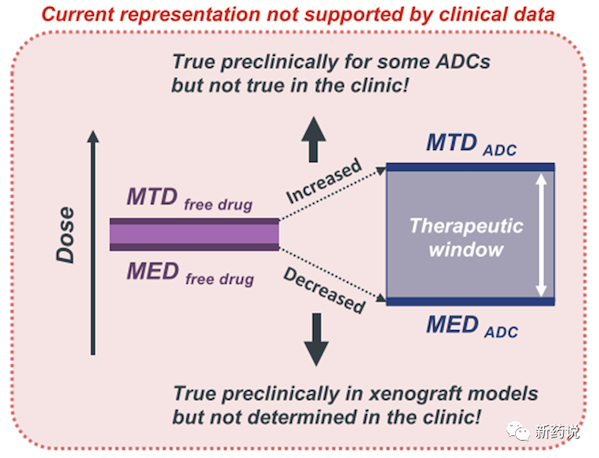
既然概念是清晰的,是不是就有一个疑惑,为什么看到的数据从来都是和阳性药去比扩大了几倍,而没看到过安全窗口到底是几(比如8.5或者20)的这种数值呢?
02 ds8201临床爬坡是怎么设计的?
在此仔细翻了ds8201的数据,我们用这个经典产品来说说安全窗口是几这个问题,先看看它临床爬坡是怎么设计以及怎么爬的。
在食蟹猴上,8201 hnstd为30mg/kg,换算到人则为9.7 mg/kg,取了这个剂量的1/12即0.8 mg/kg作为爬坡起始剂量。
然后看一下爬坡结果:
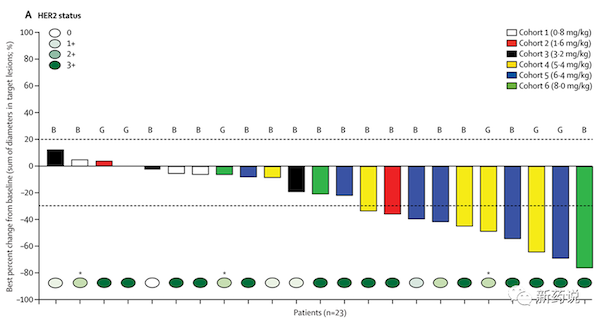
可以看到,1.6 mg/kg时,有1例病人出现了pr,但是3.2 mg/kg的3例病人都未出现pr,接下来便是pr2d的5.4 mg/kg了,而mtd为8 mg/kg。
那么这个时候med能不能按1.6 mg/kg算就不好说了,如果可以,安全窗口是5,如果不能,则只能按照5.4mg/kg算,此时安全窗口是1.5。
鉴于3.2 mg/kg的3例病人的ihc染色都为0,做不出pr可能也正常,所以med应该在1.6 -5.4mg/kg中间,这样看的话,ds8201安全窗口肯定大于1.5,最大为5。
但肯定不是所有药都做完i期再看安全窗,pre-clinical阶段数据怎么来看呢?有用鼠的有效剂量和鼠的耐受剂量算的;但更多的相对更准确的,是用鼠的有效剂量和猴的hnstd(highest non-servicely toxic dose,最高非毒性剂量)的比值来算,所以经常看到,临床前数据的表述为“小鼠cdx或者pdx模型上药效和8201的相当,但是猴子更耐受,所以安全窗比它大了几倍 ”。
有道理吗?只要数据真实,其实是可以的。那这个数据真实怎么判定呢?思考一下里面的逻辑,比如抗体亲和力如何、表位有没有关系、linker稳定性、payload毒性,去比一比,如果有道理则能理解,如果完全说不通,那么这个hnstd的数值准不准则需要考量。
03 hnstd或者mtd 决定给药上限那么这个是靶点导致的还是毒素掉落导致的呢?
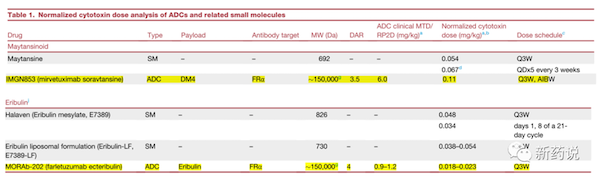
然后,就是一个比较有意思的现象,即free drug的mtd值,和adc normalized payload的mtd/rp2d值水平整体相当。

简单来说就是,如果用的mmae的payload, 临床给药周期都归一化到q3w,normalized payload的量最后都集中在一个范围里,大致范围在0.05mg/kg上下。
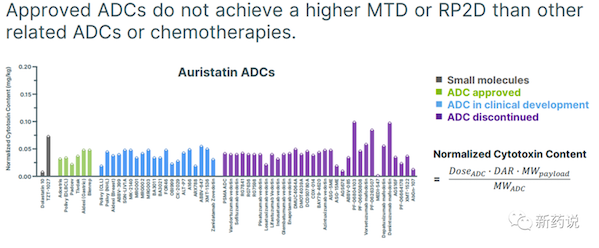
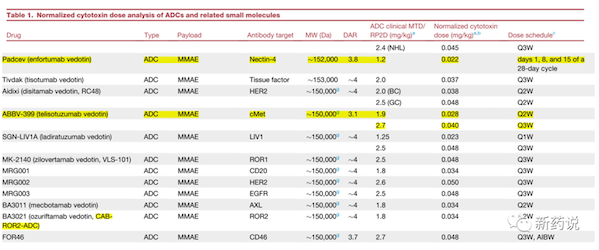
这个角度看,安全性肯定是和血浆中掉落的payload的量或者payload的代谢是有关系的,否则,不会出现不同靶点之间按照毒素类别来分rp2d or mtd的剂量。
那么如果payload定了,linker不是奇奇怪怪的比如immu132这种的,安全性跟靶点关系如何呢?
这里还是找两个linker-payload、 dar值和偶联技术完全一样但是靶点不同的两个产品来看,比如第一三共的ds1062 (trop2 adc, ggfg-dxd, dar4)和ds7300 (b7h3 adc, ggfg-dxd, dar4)。
表达上看,b7h3是比trop2干净的;
临床前食蟹猴的hnstdtrop2靶点的ds1062为10mg/kg, b7h3靶点的ds7300 为30mg/kg;
临床爬坡b7h3也爬的比trop2好很多, b7h3的rp2d在8-12mg/kg之间,高于trop2 的rp2d为6mg/kg,normalize到payload以后,和her2 dxd相当。
所以,linker-payload端确定以后,安全性和靶点以及抗体的亲和力肯定是有关系。以上都说的是安全性,即能接受剂量的上限问题,med是另外一个话题了。
04 2023年aacr会议,zymeworks最近公布数据
其发表了一个摘要编号为1538的poster,在上述paper基础上,又讨论了linker稳定性与临床效果的关系,指出临床前linker稳定性的数据并不能很好地反映临床效果,拿enhertu为例,人体的payload auc/总抗auc数值除以猴子的payload auc/总抗auc数值,等于21.6;这个值在mmae上面更高,几个mmae的产品,人体的payload auc/总抗auc数值除以猴子的payload auc/总抗auc数值,从95倍-260倍不等。
这个里面的科学问题扎进去细究应该是有很多门道,但是要不要很纠结在这个点上,怎么说呢,我自己觉得,只要你不是fic的产品,就跟安全窗口这件事情一样,和前面的产品去对比,还是有说服力的;如果是fic的产品,可能小鼠med和猴hnstd的值会反映的更直接一些。只是hnstd因为猴子的问题,剂量跨度往往比较大,不能做到很准确的数值,所以两个结合起来分析更明确一些。
做一个类比,比如抗体开发的时候,很怕遇到的风险之一为抗体的非特异结合,即off target时,而这种off target其实很多时候能通过鼠的pk去反应出来,如果药效和pk没有异常,那大概率off target 是没有问题的,很多抗体开发的时候都是因为药效异常然后发现是pk异常引起的,这个好理解,然后再往回去深究,发现是因为非特异的结合了其他靶点。所以总的就是,看数据不用只纠结一个点,动态平衡的去看。
小结
一直说安全窗口这个事情,有时候并没有那么仔细的审视过,本篇以ds8201为例说明了安全窗口如何计算,以及临床前如何去表述所开发产品的安全窗口。另外,关于毒性是源自毒素还是靶点,根据数据去做了一些梳理,感觉先跟毒素有关,毒素确定,跟靶点相关。至于偶联方式,比如定点偶联这种的能改善多少,感觉目前数据还是不够多,可能再攒攒临床数据总结起来能更明朗一些吧。
另外,adc大家的目光越来越聚集在安全性上了,但是分析数据的时候也不能被带偏,只看mtd不考虑med,或者只看med的数据(比如拿一个mmae去和dxd比药效)不考虑mtd都是不合适的。
参考文献1. safety, pharmacokinetics, and antitumour activity of trastuzumab deruxtecan (ds-8201), a her2-targeting antibody–drug conjugate, in patients with advanced breast and gastric or gastro-oesophageal tumours: a phase 1 dose-escalation study, the lancet oncology, 2017.2. the therapeutic window of antibody drug conjugates: a dogma in need of revision, cancer cell, 2022.3. revisiting the dogma of antibody drug conjugates (adcs): emerging data challenge the benefit of linker stability and the primacy of payload delivery, abstract #1538 , 2023 aacr
责编: editor
相关news
- 55 湖北 康华生物(300841.sz)近日披露公告,拟采取增资、受让等方式分期将纳美信(上海)生物科技有限公司(简称“纳美信”)100%股权纳入麾下,以此获得完整的mrna技术平台,完善公司生物医药产业战略布局。 “这笔交易本质上是地方国资利用上市公司平台进行mrna疫苗产业布局。”2月1日,北京一位医药专业人士告诉《经济参考报》记者,尽管交易方案设置了投资风险对冲措施,但这笔交易有两大风险不可小觑:一是lnp(脂质纳米颗粒)专利是mrna产业化的核心“卡脖子”环节,lnp专利由加拿大arbutus等国际巨头掌控,若纳美信无法突破,整个投资逻辑将崩塌;二是mrna技术从疫苗走向肿瘤治疗的最大障碍——lnp的“肝脏陷阱”和组织靶向性缺失。 专利问题成投资成败关键 根据公告,康华生物此次交易将视纳美信的临床试验情况分三期进行收购(与里程碑绑定),对应的当期的纳美信投前估值分别不超过3.2亿元、4.4亿元、8.3亿元。第一期康华生物拟斥资1.2亿元认购741万元纳美信新增注册资本,增资完成后持有纳美信27.2727%股权。康华生物向纳美信支付意向金2000万元。若纳美信rsv疫苗临床数据不佳,则康华生物首期投资可能“打水漂”(失去控制权,无法并表)。 康华生物入局mrna赛道,注定要走一段艰难路,此前以身入局者,大多铩羽而归。 时间拉回2020年,全球mrna疫苗大获成功,资本疯狂涌入。国产mrna三剑客(斯微生物、艾博生物、丽凡达生物)之一的斯微生物凭借“mrna全链条技术平台”和“lpp递送系统全球独家专利”的故事,成为资本宠儿。从2020年到2023年,短短三年多时间,斯微生物完成多轮融资,累计金额超13亿元,投资方包括红杉中国、药明康德、景林投资、招商健康等顶级机构,估值一度达到70亿元。但终因技术难以商业化、资金链断裂等因素,斯微生物2024年6月被法院裁定受理破产清算。此外,沃森生物(300142.sz)曾投资的估值最高达190亿元的艾博生物、艾美疫苗(06660.hk)重金收购的丽凡达生物,最终均以失败告终。 国产mrna三剑客落败,一个重要的原因就是技术代差较大,三家公司虽路径不同,但均面临海外专利墙与临床验证资源不足的共同难题。mrna药物研发的关键在于序列设计和递送系统。mrna药物研发就像“放风筝”,序列设计是风筝本身的骨架和材质,递送系统lnp是牵着风筝的线——线断了或风筝破了,都飞不起来。由于国外药企在mrna技术上较早投入了大量的资源研发,因此在源头创新、递送系统、产业链、临床验证、全球化能力五个层面优势明显。以lnp专利为例,arbutus/genevant掌握的早期lnp专利对特定阳离子脂质结构和配比形成较高壁垒,后来者需设计全新脂质或支付专利许可费,才能降低侵权风险。 纳美信在凯发k8天生赢家一触即发官网宣称具有自主知识产权的非编码区序列和密码子优化算法,基于ai、deeplearning的抗原设计和优化,circrna纯化工艺、lnp冻干工艺等方面突破行业技术难点。这些描述的技术优势均集中在递送系统的外围优化,对最核心的阳离子脂质结构创新只字未提。投资者无法从公开信息判断纳美信能否越过lnp专利壁垒。相反,威斯津生物、荣灿生物等公司则明确宣称其突破了lnp全球专利壁垒。 康华生物称,纳美信是一家专注于mrna领域新型疫苗与药物研发的生物科技企业,已构建覆盖“序列设计-递送系统-生产工艺”的全链条mrna药物技术体系。 从研发管线来看,纳美信主要聚焦呼吸道合胞病毒(rsv)、单纯疱疹病毒(hsv)临床刚需,布局代谢疾病、肿瘤等治疗领域。目前,纳美信自主研发的冻干剂型呼吸道合胞病毒mrna疫苗已进入i期临床试验阶段。 尽管纳美信有意利用mrna技术布局肿瘤等治疗领域,但却无法回避mrna技术应用的核心矛盾——lnp递送系统的“肝脏陷阱”构成了从疫苗升级到治疗性药物的不可逾越的结构性壁垒。这也是为什么mrna技术基本都应用于靶向性要求较低的疫苗开发,而不是对靶向性、精度要求更高的肿瘤治疗药物开发。换言之,mrna治疗领域的门槛,不是“有钱就能砸出来”,而是需要在lnp靶向性上实现从0到1的原始创新。没有这项技术,所有关于“免疫治疗”的故事都难以变成现实。 纳美信在凯发k8天生赢家一触即发官网中称,该公司将利用mrna技术平台优势,重点解决现有技术急需改进或没有上市产品的疫苗、免疫治疗品种的问题, 但其技术描述完全回避了靶向递送这一核心问题。 据媒体报道,纳美信计划在2026年推动rsv疫苗进入ⅱ期临床,并继续深耕hsv等新管线。更长远的目标,是从生物学机制出发,通过源头创新,利用mrna技术平台优势,解决未成药、难成药的临床痛点问题,真正实现创新平台、创新研发、普惠新药。 要实现上述目标,纳美信需要投入大量资金进行研发。 地方国资或“一箭多雕” 此次投资纳美信,被业界视为地方国资借助上市公司孵化疫苗业务之举。 地方国资与康华生物的关系是2025年7月21日公之于众的。康华生物原控股股东、实际控制人王振滔采取“股份协议转让 表决权委托”的方式将康华生物控制权转让给上海万可欣生物科技合伙企业(有限合伙)(简称“万可欣生物”)。其中,股份转让对价为18.51亿元(每股65.0266元、2846.6638万股)。万可欣生物成为康华生物控股股东,其执行事务合伙人是上海上实生物医药管理咨询有限公司(简称“上海上实医药”),由于上海上实医药不存在单一股东能控制其股东会及董事会的情形,故上海上实医药无实际控制人,因此万可欣生物亦无实际控制人。 然而,万可欣生物两大lp中,上海医药(集团)有限公司持股19.79%,其实际控制人为上海国资委;上海生物医药并购私募基金合伙企业(有限合伙)持股80.209%,该基金穿透后lp则有上海医药(601607.sh)、上海张江创投等众多国资平台。万可欣生物入主康华生物后,于2025年11月改选了上市公司董事会。 北京某私募股权投资机构部门负责人告诉记者,康华生物是上海生物医药并购基金的首个控股项目,肩负着探索“国资基金并购整合新模式”的使命,其角色是上海生物医药特别是疫苗产业的孵化整合平台。万可欣生物入主之时,市场就高度关注其整合节奏。 从改组董事会到出手投资纳美信,上海生物医药并购基金动作迅速。在业界人士看来,康华生物投资纳美信,地方国资“一箭多雕”:一是进一步提高纳美信的资金储备,为后续研发投入提供充足弹药;二是拓宽纳美信的融资渠道,分散原有股东投资风险,进一步提升纳美信整体估值;三是通过分期投资纳美信,康华生物拓宽技术、产品管线,以实现公司转型升级。 然而,地方国资通过分期付款、里程碑绑定、对赌兜底等结构,确实构建了“风险隔离、估值跃升、平台整合”的多重意图,但其根基建立在纳美信的lnp递送技术上。这一关键信息却又是康华生物未充分披露的风险之处。 更为关键的是,康华生物自身正遭遇发展困境。公司产品结构单一,大部分营收依赖狂犬病疫苗单一品种,缺乏第二增长曲线,由于疫苗集采及价格管控趋严、竞品迭出,公司2020年上市,2021年净利达到峰值后便一路下滑。2025年,公司预计归属于上市公司股东的净利润为1.91亿—2.33亿元,较2024年下降41.55%—52.09%。业绩下滑主要原因是受行业政策调整、市场竞争等因素影响,公司疫苗销售收入较上年同期下降约11%,销售利润率有所下降;公司重组六价诺如病毒疫苗未获得海外许可收入。 此外,万可欣生物入主之时,还曾订立对赌协议,约定康华生物在2025年度及2026年度(“承诺期”)内经审计的扣除非经常性损益后归属于母公司所有者的净利润合计数不低于7.28亿元;且承诺期内2025年度及2026年度研发费用合计不低于2.6亿元。 若按照2025年的业绩预告测算,则康华生物2026年的扣非净利润应在4.98亿—5.20亿元。以康华生物当下的境况来看,投资者很难捕捉到其达标的可能信号。 本次交易构成关联交易,康华生物需在签署意向协议生效后三个交易日向纳美信缴纳2000万元意向金。公司称,纳美信拥有完整的mrna技术平台,如本次交易后续实质性推进,将进一步完善公司生物医药产业战略布局,加速前沿技术平台建设,提升核心竞争力,同时此次交易有利于发挥公司与纳美信在研发、临床、生产及商业化方面的协同效应,加速在研品种产业化进程,优化资源配置效率。 “尽管是分期交易,但康华生物是在做一项风险投资。”2月2日,四川资本圈一位专业从事资本运作的财务人士表示,纳美信的研发管线尚处临床早期,更适合在基金孵化器中培育更为成熟后,再拉康华生物入股。考虑到万可欣生物是运用杠杆资金收购康华生物控制权、康华生物近期二级市场表现低迷,康华生物此次投资纳美信的真实动机值得投资者仔细甄别。 2026-02-06
- 接轨国际!艾迪药业拿下坦桑尼亚ml3级gmp认证 2026-02-05
- 石药集团氯维地平乳状注射液获药品注册批件 2026-02-05
- 派林生物:人凝血因子ix药品注册上市许可获受理 2026-02-05
- 翰思艾泰:hx111完成i期临床首例患者给药 2026-02-05
您已成功订阅,无需重复提交。
确认
邮件订阅
请输入正确邮箱!
订阅
邮件订阅热门医贸资讯,了解第一手信息。
行业动态更多
-
-
接轨国际!艾迪药业拿下坦桑尼亚ml3级gmp认证
2026-02-05 -
石药集团氯维地平乳状注射液获药品注册批件
2026-02-05 -
派林生物:人凝血因子ix药品注册上市许可获受理
2026-02-05