 对于在东南亚进行药品注册的药企来说,泰国绝对算是难攻破的市场了。如果只是说产品注册资料繁杂,还不足以撼动大家注册的决心。那究竟是什么样子的门槛和要求,使得国内药企对于这个市场又爱又恨呢?
对于在东南亚进行药品注册的药企来说,泰国绝对算是难攻破的市场了。如果只是说产品注册资料繁杂,还不足以撼动大家注册的决心。那究竟是什么样子的门槛和要求,使得国内药企对于这个市场又爱又恨呢?
根据泰国卫生部规定,在申请药品注册之前,所有的海外药品生产商都必须先进行gmp资质认证,通过认证之后方可递交产品注册资料。从去年开始,就有消息传出泰国卫生部将会针对gmp资质认证颁布新的法规。今年6月,最新的gmp资质认证要求终于在千呼万唤中出来了。
泰国作为pic/s成员国之一,对于其他pic/s成员国和非成员国的gmp资质认证的要求也有所不同。根据生产企业所在的国家和地区具体来说可以分为三大类:
1. pic/s成员国;
2. 非成员国,但有pic/s成员所颁发的gmp证书;
3. 非成员国,且无pic/s成员所颁发的gmp证书。
小d带大家来详细解析一下,具体要求有哪些:
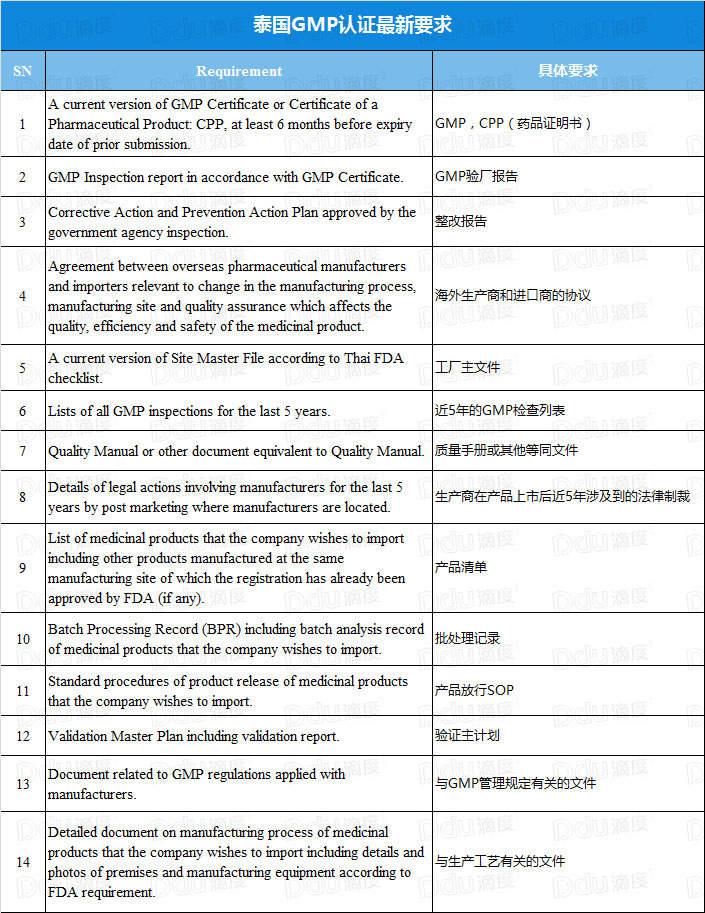
根据生产企业所在地,结合以上列表中提到的要求,可以归纳为以下:
ic/s成员:仅需提供列表中的1-4点内容;
非成员,但有pic/s成员所颁发的gmp证书:需要提供1-5点内容;
非成员国,且无pic/s成员所颁发的gmp证书:需要提供列表中提到的所有内容。
详细研究完列表中的14点要求,小d心里也忍不住抖了一下,都是生产药品的企业,要求却天差地别。不过大家也不要太灰心,近年来国内药企gmp水平和资料的不断完善,拿下泰国市场也不是没有可能的。
以上便是对于泰国gmp资质认证的简要介绍。作为全球跨境医贸b2b电子商务平台,将实时关注tfda(泰国卫生部)产品注册要求的最新动态,为每一位辛苦的海外拓荒者带来最新鲜最实用的资讯。
责编: daisy
相关news
- 滴度学院:菲律宾药品gmp认证流程和要求 2018-03-16
- 敲黑板!2018年6大政策冲击,影响众多药企 2018-02-27
- 助力跨境医贸 滴度与瑞士sgs合作推出资质认证服务 2017-08-22
- 滴度与瑞士sgs强强联手 推出资质认证服务 2017-08-18
- 有人@你 | 史上医贸干货最多的发布会 2017-08-07
 4,027
4,027